ブライトパス・バイオ永井健一代表に聞く〜がん免疫治療により自らの免疫力でがんを克服する世界の実現

オプジーボをはじめとする免疫チェックポイント阻害薬の登場により、新たな時代に入ったとされる「がん免疫療法」。手術・抗がん剤・放射線の三大がん治療に加わる“第4のがん治療”として注目される一方で、治療成績の良好な皮膚がんでも効果が認められるがん患者は約30%に過ぎず、その効果も個人差が大きいという。加えて、予測しづらい副作用や高額な治療費も克服すべき課題だ。これに対し「科学的根拠に基づいた多面的なアプローチでがん免疫の新領域を切り開きたい」というのが、ブライトパス・バイオ株式会社(東証マザーズ4594)代表取締役社長の永井健一氏だ。がんワクチンの創薬から始まった同社は、細胞医薬や抗体医薬の分野にもパイプライン(開発品群)を広げ、がん免疫サイクルに着目した新規がん免疫治療薬の開発に取り組む。がん免疫治療薬は果たして、がん治療にパラダイムシフトを起こせるのか。創業や上場の経緯、展望などもあわせて、がん免疫治療薬の現在地を伺った。
がんワクチン・細胞・抗体の相乗的な効果で開発を加速化

-はじめに、事業内容をお聞かせください。
当社は「一人ひとりが、免疫という自らの力で、がんを克服する世界を実現する」ことを目指している、新規のがん免疫治療薬の開発に特化した創薬ベンチャーです。
近年、免疫チェックポイント阻害抗体の研究が進み、免疫機能を活性化させてがんを排除するという創薬コンセプトの有効性が証明されてきました。当社ががん免疫治療薬にフォーカスする理由は、この創薬コンセプトを実現することで、従来の治療法では治療効果が得られなかった医療ニーズに対し、革新的なソリューションが提供できるフロンティアがあると考えるからです。それがまさに、当社が創業以来取り組んで来た経験とノウハウの蓄積が活かせ、世界の医薬品市場の成長をリードできる領域でもあります。
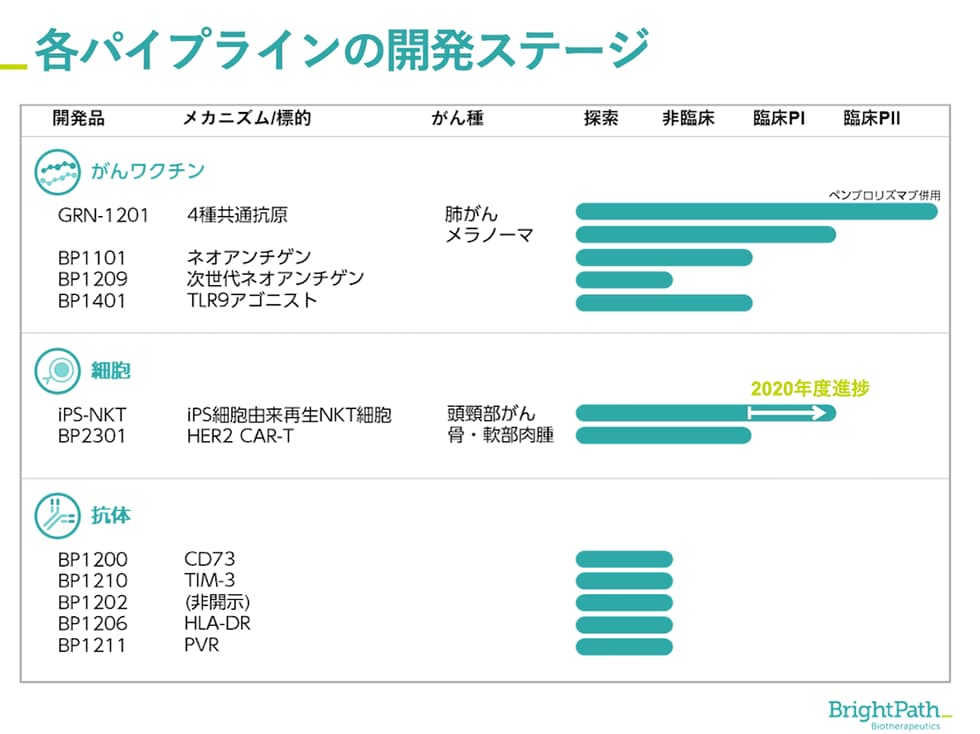
当社が開発を手掛ける新規がん免疫治療薬のモダリティ(医薬品形態)は、主に「がんワクチン・細胞・抗体」の3つです。がんペプチドワクチン「GRN-1201」は、現在、非小細胞肺がんを対象に免疫チェックポイント阻害剤との併用による第二相臨床試験を米国で進めています。それに続き「iPS-NKT(iPS細胞由来再生NKT細胞療法)」でも頭頸部がんを対象とする臨床試験が始まりました。このほかにも、各種の固形がんを対象に複数の探索・非臨床試験ステージのパイプラインを有しています。
探索研究から早期臨床試験段階にある複数のモダリティのパイプラインによる相乗効果によって、開発を加速化し、早期に臨床試験が可能なパイプラインをさらに拡充させていく予定です。
2000年代初頭に訪れた日本のバイオテクノロジー黎明期

-遡って、創業の背景を教えてください。
当社の事業は、元久留米大学医学部の伊東恭悟教授らが1992年から始めた、がんペプチドワクチンの基礎研究および臨床研究の成果を承継したことからスタートしました。いわゆるアカデミアシーズを企業シーズに変えて育てていこうという使命のもと、大学の研究成果を、医薬品としての承認、そして上市につなげるために必要な臨床試験を推進する会社として、2003年に設立されたのが当社です。
昨今では、ウイルスに感染した細胞やがん細胞を直接殺傷する「キラーT細胞」という言葉をよく耳にするようになりました。そのキラーT細胞が敵として認識する目印が、ごく小さなタンパク質の断片であるペプチドだということが、1991年に発見されました。翌年から伊東恭悟教授らが進めた研究により、久留米大学が嚆矢となって本邦ではがんペプチドワクチンの開発が急速に広がっていったのです。
残念ながら、創業時のモダリティである「ITK-1」というがんペプチドワクチンは、第三相試験という承認の手前の臨床試験まで進んだものの、統計的有意差をもって有効性を示せずに開発がストップしました。しかし、そこで得た治験やノウハウを活かして、次のモダリティの開発に取り組んでいます。
-永井社長は2009年にジョインされたと伺いました。どのような背景があったのですか?
メリルリンチ日本証券株式会社の投資銀行部門で主にM&Aのアドバイザリー業務を9年弱経験しました。バイオベンチャーに転身したのはそこからです。メリルリンチ時代の先輩がいたこともあり、2005年に株式会社ペルセウスプロテオミクスへCFOとしてジョインしました。同社は富士フイルムの傘下に入ったため、2009年に当社の前身である株式会社グリーンペプタイドに参画。CFOを1年半ほど経た後、新しい領域を開発するミッションを担い、前社長を引き継ぐ形で社長に就任したという流れです。
-なぜバイオベンチャーの世界に飛び込もうとお考えになったのですか?
私がメリルリンチにいた1998年は、日本経済とって大きな転換点がいくつもありました。日本の金融業界の再編が加速する一方で、新しい産業が勃興するのを目の当たりにするうちに、黎明期の業界で活躍してみたいと考えるようになったのです。その中でも、とくに興味を持ったのがバイオテクノロジー分野です。
日本のバイオテクノロジーは、法制度の面でも世界に20年ほど遅れを取っていた印象がありました。それが、いわゆる日本版バイ・ドール制度である、1999年の産業活力再生特別措置法の施行や、2001年の大学発ベンチャー1,000社計画の発表などにより急激に産業の転換点を迎えることとなりました。私は日本のバイオ産業がこれから急速に発展するだろうと見込んでいたのです。
加えて、ゼロからイチの新しい価値を生み出す事業にも魅力を感じていました。私自身、サイエンティストではありませんが、そうした新たな価値を創造する事業に少しでも関わりたいという意識が強かったのです。
老舗バイオベンチャーとしての上場までの道のり

-上場は就任当初から考えられていたのでしょうか。
上場を決意したのは2012年の後半です。創業以来、いわゆる“一本足打法”で進めてきたがんペプチドワクチン「ITK-1」を富士フイルム株式会社へライセンスアウトし、当社では次のステージを見据えた新規パイプラインの創製にチャレンジしようという機運が高まっていました。そこに、VCのイグジットの期待などさまざまな要因が重なったこともあり、私たちが進むべき道はIPOだろうと判断したのです。
-上場までの道のりでは苦労はありましたか?
最初は苦労も多かったですね。がんワクチンは患者さんによって効果の有無が分かれることがあるため、その有効性を理解してもらうのが大変でした。証券会社さん側もまだがん免疫治療薬の創薬ベンチャーを取り扱った経験が少なく、成功確率がよくわからないなど、私たちが開発するプロダクトに価値をつけてもらうことに苦労しました。
また、当時既に当社は“老舗バイオベンチャー”といわれるほど、ベンチャーとしては社歴が長く、ステークホルダーが多かったのです。そのため、上場準備を進めるにあたっては利害が錯綜することもあり「あちらを立てればこちらが立たず」で、その関係調整が大変でした。
-創薬ベンチャーは一般的に赤字先行のビジネスモデルですが、そこは論点になりませんでしたか?
大手製薬企業が開発途上にあるベンチャーのシーズをライセンスインするモデルは、米国で早くから一般的になっています。開発進捗段階に応じたライセンスの取引相場も確立されているため、ビジネスモデルそのものが論点になることはありませんでしたね。
がん免疫サイクルを正常に回すがん免疫治療薬のしくみと可能性

-さて、いよいよプロダクトの詳細を伺って参りたいと思います。現代のがん治療では、がん免疫治療薬が主流になりつつあるのですか?
私が当社に参画した2009年は、がん免疫療法によって、劇的に効果がある人がいる一方で、効かない人にはまったく効果がなく、まだまだ“暗黒大陸”といわれていた領域でした。しかし、その後のサイエンスの目覚ましい進展により、現在のがん免疫治療薬は、外科手術・放射線療法・化学療法に次ぐ「第4の治療法」としての地位を確立しています。これまでも、がん治療には約50年に一度、生存率を大きく改善する治療法の革新が起こってきましたが、がん免疫治療はまさにその革新をもたらすものといえるでしょう。
今年は新型コロナウイルス感染症の関係で感染症ワクチンが突発的に伸びていますが、医薬品産業のあらゆるカテゴリーの中で、がん治療薬の存在感は大きく増しています。がんを治療できる薬が増えてきたからに他なりませんが、その成長を担っているのが、がん免疫治療薬というわけです。従来型の外科手術、放射線療法、化学療法と組み合わせてより効果的な使われ方をするようになり、がん免疫治療薬はますます医薬品産業全体を押し上げる存在となりました。私たちは、こうしたトレンドがまだまだ続くと考えています。
-そもそも、がん免疫治療薬とはどういったものなのですか?
私たちは皆、病原菌やがん細胞を排除するための「免疫」という生体防御機構を持っています。がん細胞を排除する免疫の仕組みは「がん免疫」と呼ばれ、このがん免疫の仕組みを利用して、体の中で無秩序に異常増殖するがんを排除するのが「がん免疫療法」です。
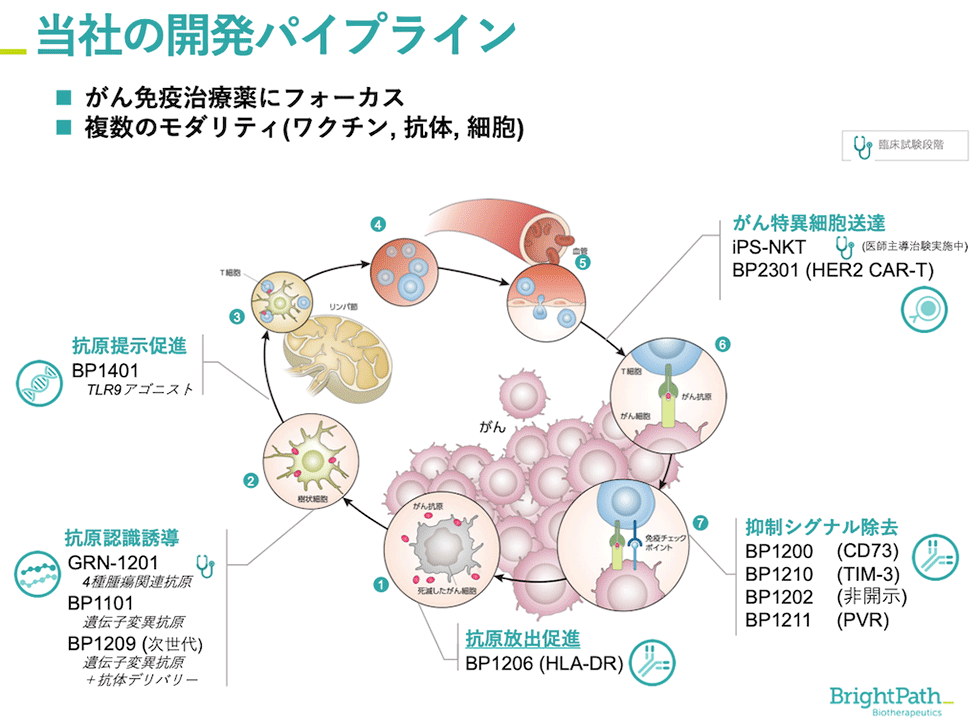
がん免疫にはサイクルがあり、7つのステップからなることが知られています。簡単にいうと、①死滅したがん細胞から抗原が放出され、②それを樹状細胞が取り込んで「がん細胞の印である同様の抗原を持つがん細胞を攻撃せよ」とT細胞に司令を出します。③攻撃モードに入ったT細胞は増殖し、④リンパ管や血管を通って⑤がん組織に入り込み、⑥T細胞の受容体ががん細胞表面の抗原と結合し、⑦最終的にがん細胞を殺傷する。そしてまた死滅したがん細胞から抗原が放出されるというサイクルです。
しかし、抗原が足りなかったり、樹状細胞がT細胞に抗原という情報を送れなかったり、T細胞がリンパ管や血管からうまく組織に入れなかったり、このサイクルのどこかで渋滞してしまうと、がん免疫サイクルがうまく回らなくなってしまうのです。こうしたがん免疫サイクルが滞る箇所は、がん種、がんのステージ、個人差などによって異なります。
当社はパイプラインにおいて複数のメカニズムやモダリティを持つことで、その滞りの解消に適した方法を選択することを可能にしており、それが強みにもなっています。そうした中で、当社では本格的な自社創製シーズの開発と他研究機関との共同研究の拠点として、2016年に川崎創薬研究所を設置しました。これにより、がんワクチンだけでなく、抗体医薬や細胞医薬の分野にも研究領域を広げています。
-細胞医薬では「iPS-NKT」の第一相試験が2020年6月に始まったそうですね。
NKT細胞は、自然免疫であるNK細胞と、抗原を獲得したT細胞の両方の性質を持った細胞です。NKT細胞はがん細胞を直接殺傷する能力をもつと同時に、ほかの免疫細胞を活性化させたり、それによって間接的にがん細胞を攻撃させたりするなど、多面的な抗腫瘍効果を持っています。つまり、がん免疫サイクルに様々な免疫細胞を動員させて回す機能がとくに優れた細胞というわけです。

しかし残念なことに、NKT細胞は血中に非常に少量しかありません。ですから、体外に取り出して、治療に必要な細胞数まで培養・増殖させることが極めて難しいという課題がありました。それにより、治療機会を逸していた患者さんがとても多かったのです。
そこで、iPS細胞技術によって、NKT細胞へ分化できる幹細胞を増殖させた後にNKT細胞へ戻すことで、治療に十分な質と量を持ったNKT細胞を確保しようというのが「iPS-NKT細胞療法(iPS細胞由来再生NKT細胞療法)」です。iPS-NKT細胞療法は「マスターセルバンク型他家細胞療法」をフォーマットとしており、診断から投与までの期間短縮や、均質な細胞の大量製造が可能になっています。
-細胞医薬のパイプラインはほかに何がありますか?
「BP2301(自家HER2 CART細胞療法)」です。これはまず、さまざまな固形がんによく見られるHER2抗原を患者さんのT細胞がきちんと認識できるように、遺伝子改変でレセプターをつけたT細胞(CAR-T細胞)を体外で増やします。それを患者さんの体内に戻すと、CAR-T細胞が体内でHER2抗原を目印にがん細胞を殺傷する、という仕組みです。

T細胞はもともと、標的が定まると標的の殺傷能力が強まり、免疫として標的排除の役割を終えた後は、そのまま残り続けて正常細胞を傷つけないよう、自死するメカニズムになっています。しかし、一定数は次の戦いに備えて、メモリー細胞(記憶細胞)として残る性質があります。このメモリーの性質をもつT細胞をCAR-T細胞療法に使えるようにしたところに当社の特徴があります。
つまり、体内で長期生存可能で、かつ持続的な抗腫瘍効果が期待できるCAR-T細胞をたくさん作れる技術を開発したというわけです。
-複数のパイプラインを同時に進めることで、がん免疫サイクルの各ステップに働きかけられるのですね。
がん免疫治療薬の究極の目的は、がん免疫サイクルを正常に回すことです。そのためには、がん免疫サイクルの主役であるキラーT細胞をどれだけ増やせるかがキーポイントとなります。
元気なT細胞を体外で作って送り込むのが細胞医薬ですし、元気なT細胞がきちんと増えるように免疫チェックポイントを調整していくのが抗体医薬、そしてがんワクチンは、T細胞にがん細胞の目印となる抗原を渡して増殖を促すものです。結局は、がん免疫サイクルで全部つながっているのです。
このように、がん免疫治療薬の領域では、どのモダリティも目指す方向は同じで、私たちは3つのモダリティに取り組んでいますので、それらを複合的に活用して、さらなるシナジー効果を狙うことができると考えています。当社が3つのモダリティに着手していることは、世界で勝負するうえでもメリットが大きいと考えています。
一人ひとりが自分の力でがんを克服できる世界を実現したい

-今後の展望を伺います。ライセンスアウトだけでなく、いずれは製薬企業への転換も視野に入れていますか?
医薬品開発は、一般的に上市まで10年以上かかり、開発後期段階になるほど多くの資金が必要になります。製薬企業になるためには、承認を取った後、さらに販売をしなければなりません。これには相当な体力が必要です。そのため当社では、新規がん免疫治療薬の探索研究から早期臨床試験までを手掛け、後期臨床試験以降は製造販売網のある製薬企業にライセンスアウトして、早期収益化を図る事業モデルを採っています。
ただ、現在のモデルでいずれかのパイプラインのライセンスアウトが成功し、開発費の負担に耐えうる資金力がついた際には、後続のパイプラインのうちいくつかは後期臨床試験以降まで進め、創薬ベンチャーから製薬企業へ転換を図っていくことも想定しています。
-がん免疫治療薬の新規開発を通して、将来的にどういう世界を作りたいとお考えですか?
がん免疫は誰もがもともと備え持っている体の機能であり、その力を後押しすることで、体の中にできたがん細胞を排除しようというのが、がん免疫治療薬です。免疫の力を適正に制御して提供することで、あらゆる人ががん治療を進めることができるのです。
これまでの治療法では、がんの根治まで成し得ることはできませんでした。また、化学療法はつらい副作用が出ることも多く、患者さんに多くの負担をかける場合もあります。私たちは、そのようながん治療のあり方を変えたいのです。がん免疫治療薬によって、一人ひとりが自分の免疫の力でがんを克服できる。そういった世界の実現に貢献したいと考えています。
-がん免疫治療薬による免疫療法は、まさに理想的な治療法といえるのですね。
その通りです。当社の社名「ブライトパス(BrightPath)」は、「ブライト=輝く」と「パス=道筋」を合わせたもので、そこには3つの思いが込められています。それは、がんの克服に取り組むすべての人達にとっての希望の光となるがん治療薬を生み出すこと。かつて暗黒大陸とまでいわれたがん免疫療法の未解明の領域に科学の光を当てること。がん免疫療法が進むべき道筋を鮮明に指し示すリーダーとなることです。
その「光」となるためには、サイエンティストたちの力を集結させることが不可欠です。がん免疫療法は科学が日進月歩で進展する領域ですので、今後も研究施設の充実やオープンイノベーションの機会拡充を図りながら、サイエンティストたちが自由闊達に開発に取り組める研究体制の構築を進めたいと思っています。
<プロフィール>
永井健一(ながい・けんいち)
ブライトパス・バイオ株式会社代表取締役社長。2011年より現任。2009年に同社取締役CFOに就任。前職は2005年より抗体医薬品シーズ開発ベンチャーの株式会社ペルセウスプロテオミクス(東証マザーズ 4882)の取締役CFOに就き、現在と合わせて10年以上の創薬ベンチャーのマネジメントを経験。その前はメリルリンチ日本証券株式会社の投資銀行部門M&Aアドバイザリーグループにて国内外のM&A案件に従事。
ブライトパス・バイオ株式会社(英文:BrightPath Biotherapeutics Co., Ltd.)
https://www.brightpathbio.com
本社事業所:東京都千代田区麹町2-2-4 麹町セントラルビル7F
川崎創薬研究所・細胞技術研究所:神奈川県川崎市川崎区殿町3-25-22 ライフイノベーションセンター
設立:2003年5月8日
資本金:5,433百万円(2020年3月31日現在)
社員数:44名(2020年3月31日現在)





